Химические свойства
Физические свойства
При обычных условиях сероводород – бесцветный газ, с сильным характерным запахом тухлых яиц. Т пл = -86 °С,Т кип = -60 °С, плохо растворим в воде, при 20 °С в 100 г воды растворяется 2,58 мл H 2 S. Очень ядовит, при вдыхании вызывает паралич, что может привести к смертельному исходу. В природе выделяется в составе вулканических газов, образуется при гниении растительных и животных организмов. Хорошо растворим в воде, при растворении образует слабую сероводородную кислоту.
- В водном растворе сероводород обладает свойствами слабой двухосновной кислоты:
H 2 S = HS - + H + ;
HS - = S 2- + H + .
- Сероводород горит в воздухе голубым пламенем. При ограниченном доступе воздуха образуется свободная сера:
2H 2 S + O 2 = 2H 2 O + 2S.
При избыточном доступе воздуха горение сероводорода приводит к образованию оксида серы (IV):
2H 2 S + 3O 2 = 2H 2 O + 2SО 2 .
- Сероводород обладает восстановительными свойствами. В зависимости от условий сероводород может окисляться в водном растворе до серы, сернистого газа и серной кислоты.
Например, он обесцвечивает бромную воду:
H 2 S + Br 2 = 2HBr + S.
взаимодействует с хлорной водой:
H 2 S + 4Cl 2 + 4H 2 O = H 2 SO 4 + 8HCl.
Струю сероводорода можно поджечь, используя диоксид свинца, так как реакция сопровождается большим выделением тепла:
3PbO 2 + 4H 2 S = 3PbS + SO 2 + 4H 2 O.
- Взаимодействие сероводорода с сернистым газом используется для получения серы из отходящих газов металлургического и сернокислого производства:
SO 2 + 2H 2 S = 3S + 2H 2 O.
С этим процессом связано образование самородной серы при вулканических процессах.
- При одновременном пропускании сернистого газа и сероводорода через раствор щелочи образуется тиосульфат:
4SO 2 + 2H 2 S + 6NaOH = 3Na 2 S 2 O 3 + 5H 2 O.
- Реакция разбавленной соляной кислоты с сульфидом железа (II)
FeS + 2HCl = FeCl 2 + H 2 S
- Взаимодействие сульфида алюминия с холодной водой
Al 2 S 3 + 6H 2 O = 2Al(OH) 3 + 3H 2 S
- Прямой синтез из элементов происходит при пропускании водорода над расплавленной серой:
H 2 + S = H 2 S.
- Нагревание смеси парафина с серой.
1.9. Сероводородная кислота и её соли
Сероводородной кислоте присущи все свойства слабых кислот. Она реагирует с металлами, оксидами металлов, основаниями.
Как двухосновная, кислота образует два типа солей – сульфиды и гидросульфиды . Гидросульфиды хорошо растворимы в воде, сульфиды щелочных и щелочно-земельных металлов также, сульфиды тяжелых металлов практически нерастворимы.
Сульфиды щелочных и щелочноземельных металлов не окрашены, остальные имеют характерную окраску, например, сульфиды меди (II), никеля и свинца – черные, кадмия, индия, олова – желтые, сурьмы – оранжевый.
Ионные сульфиды щелочных металлов M 2 S имеют структуру типа флюорита, где каждый атом серы окружен кубом из 8 атомов металла и каждый атом металла – тетраэдром из 4 атомов серы. Сульфиды типа MS характерны для щелочноземельных металлов и имеют структуру типа хлорида натрия, где каждый атом металла и серы окружен октаэдром из атомов другого сорта. При усилении ковалентного характера связи металл – сера реализуются структуры с меньшими координационными числами.
Сульфиды цветных металлов встречаются в природе как минералы и руды, служат сырьем для получения металлов.
ОПРЕДЕЛЕНИЕ
Сероводород представляет собой бесцветный газ с характерным запахом гниющего белка.
Он немного тяжелее воздуха, сжижается при температуре -60,3 o С и затвердевает при -85,6 o С. На воздухе сероводород горит голубоватым пламенем, образуя диоксид серы и воду:
2H 2 S + 3O 2 = 2H 2 O + 2SO 2 .
Если внести в пламя сероводорода какой-нибудь холодный предмет, например фарфоровую чашку, то температура пламени значительно понижается и сероводород окисляется только до свободной серы, оседающей на чашке в виде желтого налета:
2H 2 S + O 2 = 2H 2 O + 2S.
Сероводород легко воспламеняется; смесь его с воздухом взрывает. Сероводород очень ядовит. Длительное вздыхание воздуха, содержащего этот газ даже в небольших количествах, вызывает тяжелые отравления.
При 20 o С один объем воды растворяет 2,5 объема сероводорода. Раствор сероводорода в воде называется сероводородной водой. При стоянии на воздухе, особенно на свету, сероводородная воды скоро становится мутной от выделяющейся серы. Это происходит в результате окисления сероводорода кислородом воздуха.
Получение сероводорода
При высокой температуре сера взаимодействует с водородом, образуя газ сероводород.
Практически сероводород обычно получают действием разбавленных кислот на сернистые металлы, например на сульфид железа:
FeS + 2HCl = FeCl 2 + H 2 S.
Более чистый сероводород можно получитьпри гидролизе CaS, BaS или A1 2 S 3 . Чистейший газполучается прямой реакцией водорода и серы при 600 °С.
Химические свойства сероводорода
Раствор сероводорода в воде обладает свойствами кислота. Сероводород - слабая двухосновная кислота. Она диссоциирует ступенчато и в основном по первой ступени:
H 2 S↔H + + HS — (K 1 = 6×10 -8).
Диссоциация по второй ступени
HS — ↔H + + S 2- (K 2 = 10 -14)
протекает в ничтожно малой степени.
Сероводород - сильный восстановитель. При действии сильных окислителей он окисляется до диоксида серы или до серной кислоты; глубина окисления зависит от условий: температуры, рН раствора, концентрации окислителя. Например, реакция с хлором обычно протекает до образования серной кислоты:
H 2 S + 4Cl 2 + 4H 2 O = H 2 SO 4 + 8HCl.
Средние соли сероводорода называют сульфидами.
Применение сероводорода
Применение сероводорода довольно ограничено, что, в первую очередь связано с его высокой токсичностью. Он нашел применение в лабораторной практике в качестве осадителя тяжелых металлов. Сероводород служит сырьем для получения серной кислоты, серы в элементарном виде и сульфидов
Примеры решения задач
ПРИМЕР 1
| Задание | Определите во сколько раз тяжелее воздуха сероводород H 2 S. |
| Решение | Отношение массы данного газа к массе другого газа, взятого в том же объеме, при той же температуре и том же давлении, называется относительной плотностью первого газа по второму. Данная величина показывает, во сколько раз первый газ тяжелее или легче второго газа.
Относительную молекулярную массу воздуха принимают равной 29 (с учетом содержания в воздухе азота, кислорода и других газов). Следует отметить, что понятие «относительная молекулярная масса воздуха» употребляется условно, так как воздух - это смесь газов. D air (H 2 S) = M r (H 2 S) / M r (air); D air (H 2 S) = 34 / 29 = 1,17. M r (H 2 S) = 2 ×A r (H) + A r (S) = 2 × 1 + 32 = 2 + 32 = 34. |
| Ответ | Сероводород H 2 S тяжелее воздуха в 1,17 раз. |
ПРИМЕР 2
| Задание | Найдите плотность по водороду смеси газов, в которой объемная доля кислорода составляет 20%, водорода - 40%, остальное - сероводород H 2 S. |
| Решение | Объемные доли газов будут совпадать с молярными, т.е. с долями количеств веществ, это следствие из закона Авогадро. Найдем условную молекулярную массу смеси:
M r conditional (mixture) = φ (O 2) ×M r (O 2) + φ (H 2) ×M r (H 2) + φ (H 2 S) ×M r (H 2 S); |
- (сернистый водород) H2S, бесцветный газ с запахом тухлых яиц; tпл?85,54 .С, tкип?60,35 .С; при 0 .С сжижается под давлением 1 МПа. Восстановитель. Побочный продукт при очистке нефтепродуктов, коксовании угля и др.; образуется при разложении… … Большой Энциклопедический словарь
СЕРОВОДОРОД - (H2S), бесцветный, ядовитый газ с запахом тухлых яиц. Образуется в процессах гниения, содержится в сырой нефти. Получают действием серной кислоты на сульфиды металлов. Используется в традиционном КАЧЕСТВЕННОМ АНАЛИЗЕ. Свойства: температура… … Научно-технический энциклопедический словарь
СЕРОВОДОРОД - СЕРОВОДОРОД, сероводорода, мн. нет, муж. (хим.). Газ, образующийся при гниении белковых веществ, издающий запах тухлых яиц. Толковый словарь Ушакова. Д.Н. Ушаков. 1935 1940 … Толковый словарь Ушакова
СЕРОВОДОРОД - СЕРОВОДОРОД, а, муж. Бесцветный газ с резким неприятным запахом, образующийся при разложении белковых веществ. | прил. сероводородный, ая, ое. Толковый словарь Ожегова. С.И. Ожегов, Н.Ю. Шведова. 1949 1992 … Толковый словарь Ожегова
сероводород - сущ., кол во синонимов: 1 газ (55) Словарь синонимов ASIS. В.Н. Тришин. 2013 … Словарь синонимов
СЕРОВОДОРОД - бесцветный ядовитый газ H2S с неприятным специфическим запахом. Обладает слабокислотными свойствами. 1 л С. при t 0 °C и давлении 760 мм составляет 1,539 г. Встречается в нефтях, в природных водах, в газах биохимического происхождения, как… … Геологическая энциклопедия
СЕРОВОДОРОД - СЕРОВОДОРОД, H2S (молекулярный вес 34,07), бесцветный газ с характерным запахом тухлых яиц. Литр газа при нормальных условиях (0°, 760 мм) весит 1,5392 г. Темп, кипения 62°, плавления 83°; С. входит в состав газообразных выделений… … Большая медицинская энциклопедия
сероводород - — Тематики биотехнологии EN hydrogen sulfide … Справочник технического переводчика
сероводород - СЕРОВОДОРОД, а, м Бесцветный газ с резким неприятным запахом, образующийся при разложении белковых веществ и представляющий собой соединение серы с водородом. Сероводород содержится в некоторых минеральных водах и лечебных грязях и используется… … Толковый словарь русских существительных
Книги
- Как бросить курить! (DVD) , Пелинский Игорь , "Нет ничего легче, чем бросить курить, - я уже тридцать раз бросал" (Марк Твен). Почему люди начинают курить? Чтобы расслабиться, отвлечься, собраться с мыслями, избавиться от стресса или… Категория: Психология. Бизнес Серия: Путь к здоровью и совершенству Издатель: Сова-Фильм , Купить за 275 руб
- Вестиментиферы – бескишечные беспозвоночные морских глубин , В. В. Малахов , Монография посвящена новой группе гигантских (до 2,5 м) глубоководных животных, обитающих в районах глубоководной гидротермальной активности и холодных углеводородных просачиваний. Наиболее… Категория: Медицина Издатель: Товарищество научных изданий КМК , Купить за 176 руб электронная книга (fb2, fb3, epub, mobi, pdf, html, pdb, lit, doc, rtf, txt)
О.С.ЗАЙЦЕВ
УЧЕБНАЯ КНИГА ПО ХИМИИ
ДЛЯ УЧИТЕЛЕЙ СРЕДНИХ ШКОЛ,
СТУДЕНТОВ ПЕДАГОГИЧЕСКИХ ВУЗОВ И ШКОЛЬНИКОВ 9–10
КЛАССОВ,
РЕШИВШИХ ПОСВЯТИТЬ СЕБЯ ХИМИИ И ЕСТЕСТВОЗНАНИЮ
УЧЕБНИКЗАДАЧНИКЛАБОРАТОРНЫЙ ПРАКТИКУМНАУЧНЫЕ РАССКАЗЫ ДЛЯ ЧТЕНИЯ
Продолжение. См. № 4–14, 16–28, 30–34, 37–44, 47,
48/2002;
1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23,
24, 25-26, 27-28, 29, 30, 31, 32, 35, 36, 37, 39, 41, 42, 43, 44 , 46, 47/2003;
1, 2, 3, 4, 5, 7, 11, 13, 14, 16, 17, 20, 22, 24/2004
§ 8.1. Окислительно-восстановительные реакции
ЛАБОРАТОРНЫЕ ИССЛЕДОВАНИЯ
(продолжение)
2. Озон – окислитель.
Озон – важнейшее для природы и человека вещество.
Озон создает вокруг Земли на высоте от 10 до 50 км озоносферу с максимумом содержания озона на высоте 20–25 км. Находясь в верхних слоях атмосферы, озон не пропускает к поверхности Земли большую часть ультрафиолетовых лучей Солнца, губительно действующих на человека, животный и растительный мир. В последние годы обнаружены участки озоносферы с сильно пониженным содержанием озона, так называемые озоновые дыры. Неизвестно, образовывались ли озоновые дыры раньше. Также непонятны и причины их возникновения. Предполагают, что хлорсодержащие фреоны холодильников и парфюмерных баллончиков под действием ультрафиолетового излучения Солнца выделяют атомы хлора, которые реагируют с озоном и тем самым уменьшают его концентрацию в верхних слоях атмосферы. Опасность озоновых дыр в атмосфере крайне беспокоит ученых.
В нижних слоях атмосферы озон образуется в результате ряда последовательных реакций между кислородом воздуха и оксидами азота, выбрасываемыми плохо отрегулированными двигателями автомобилей и создающимися разрядами высоковольтных линий электропередач. Озон очень вреден для дыхания – он разрушает ткани бронхов и легких. Озон чрезвычайно ядовит (сильнее угарного газа). Предельно допустимая концентрация в воздухе – 10 –5 %.
Таким образом, озон в верхних и в нижних слоях атмосферы оказывает противоположное по своим результатам воздействие на человека и животный мир.
Озон наряду с хлором используют для обработки воды, чтобы разрушить органические примеси и уничтожить бактерии. Однако как хлорирование, так и озонирование воды имеет свои преимущества и недостатки. При хлорировании воды уничтожаются практически полностью бактерии, но образуются вредные для здоровья органические вещества канцерогенного характера (способствуют развитию раковых опухолей) – диоксины и подобные им соединения. При озонировании воды такие вещества не образуются, но озон убивает не все бактерии, и оставшиеся живыми бактерии через некоторое время обильно размножаются, поглощая остатки убитых бактерий, и вода становится даже более загрязненной бактериальной флорой. Поэтому озонирование питьевой воды лучше применять при ее быстром использовании. Очень эффективно озонирование воды в бассейнах, когда вода непрерывно циркулирует через озонатор. Озон применяют также и для очистки воздуха. Он относится к числу экологически чистых окислителей, не оставляющих вредных продуктов своего распада.
Озон окисляет почти все металлы, кроме золота и металлов платиновой группы.
Химические способы получения озона неэффективны или слишком опасны. Поэтому советуем вам получить озон в смеси с воздухом в озонаторе (действие слабого электрического разряда на кислород), имеющемся в школьной физической лаборатории.
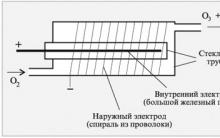
Озон чаще всего получают действием на газообразный кислород тихого электрического разряда (без свечения и искр), который происходит между стенками внутреннего и внешнего сосудов озонатора. Простейший озонатор нетрудно изготовить из стеклянных трубок с пробками. Как это сделать, вы поймете из рис. 8.4. Внутренний электрод – металлический стержень (длинный гвоздь), наружный электрод – проволочная спираль. Воздух можно продувать воздушным насосом для аквариума или резиновой грушей от пульверизатора. На рис. 8.4 внутренний электрод находится в стеклянной трубке (как вы думаете, почему? ), но можно собрать озонатор и без нее. Резиновые пробки быстро разъедаются озоном.
 |
Высокое напряжение удобно получить от индукционной катушки системы зажигания автомобиля, непрерывно размыкая соединение с источником низкого напряжения (аккумулятор или выпрямитель тока на 12 В).
Выход озона – несколько процентов.
Качественно обнаружить озон можно при помощи
крахмального раствора йодида калия. Этим
раствором можно пропитать полоску
фильтровальной бумаги или раствор добавить в
озонированную воду, а воздух с озоном пропускать
через раствор в пробирке. Кислород в реакцию с
йодид-ионом не вступает.
Уравнение реакции:
2I – + О 3 + Н 2 О = I 2 + O 2 + 2ОН – .
Напишите уравнения реакций приема и отдачи
электронов.
Поднесите к озонатору полоску фильтровальной
бумаги, смоченную этим раствором. (Зачем
раствор йодида калия должен содержать крахмал?)
Определению озона этим способом мешает пероксид
водорода (почему?)
.
Рассчитайте ЭДС реакции, используя электродные
потенциалы:
3. Восстановительные свойства сероводорода и сульфид-иона.
Сероводород – бесцветный газ с запахом тухлых
яиц (в состав некоторых белков входит сера).
Для проведения опытов с сероводородом можно
пользоваться газообразным сероводородом,
пропуская его через раствор с изучаемым
веществом, или приливать к исследуемым растворам
заранее приготовленную сероводородную воду (это
удобнее). Многие реакции можно проводить с
раствором сульфида натрия (реакции на
сульфид-ион S 2–).
Работать с сероводородом только под тягой! Смеси
сероводорода с воздухом сгорают со взрывом.
Сероводород обычно получают в аппарате Киппа, действуя 25%-й серной (разбавленной 1:4) или 20%-й соляной (разбавленной 1:1) кислотой на сульфид железа в виде кусочков размером 1–2 см. Уравнение реакции:
FeS (кр.) + 2Н + = Fe 2+ + H 2 S (г.).
Небольшие количества сероводорода можно получить, поместив кристаллический сульфид натрия в колбу с пробкой, через которую пропущены капельная воронка с краном и отводная трубка. Медленно приливая из воронки 5–10%-ю соляную кислоту (почему не серную?) , колбу постоянно встряхивают покачиванием, чтобы избежать местного скопления непрореагировавшей кислоты. Если этого не делать, неожиданное смешение компонентов может привести к бурной реакции, выталкиванию пробки и разрушению колбы.
Равномерный ток сероводорода получается при нагревании с серой богатых водородом органических соединений, например парафина (1 часть парафина на 1 часть серы, 300 °С).
Для получения сероводородной воды через дистиллированную воду (или прокипяченную) пропускают сероводород. В одном объеме воды растворяется около трех объемов газообразного сероводорода. При стоянии на воздухе сероводородная вода постепенно мутнеет (почему?) .
Сероводород – сильный восстановитель: галогены восстанавливаются им до галогеноводородов, серная кислота – до диоксида серы и серы.
Сероводород ядовит. Предельно допустимая концентрация в воздухе 0,01 мг/л. Даже при незначительных концентрациях сероводород раздражает глаза и дыхательные пути, вызывает головную боль. Концентрации выше 0,5 мг/л опасны для жизни. При более высоких концентрациях поражается нервная система. При вдохе сероводорода возможна остановка сердца и дыхания. Иногда сероводород скапливается в пещерах и канализационных колодцах, и попавший туда человек мгновенно теряет сознание и погибает.
В то же время сероводородные ванны оказывают лечебное действие на организм человека.
3а. Реакция сероводорода с пероксидом водорода.
Изучите действие раствора пероксида водорода
на сероводородную воду или раствор сульфида
натрия.
По результатам опытов составьте уравнения
реакций. Рассчитайте ЭДС реакции и сделайте
вывод о возможности ее прохождения.

3б. Реакция сероводорода с серной кислотой.
В пробирку с 2–3 мл сероводородной воды (или
раствора сульфида натрия) прилейте по каплям
концентрированную серную кислоту (осторожно!)
до появления мути. Что это за вещество? Какие
другие продукты могут получиться в этой реакции?
Напишите уравнения реакций. Рассчитайте ЭДС
реакции, используя электродные потенциалы:

4. Диоксид серы и сульфит-ион.
Диоксид серы, сернистый газ – важнейший загрязнитель атмосферы, выделяемый автомобильными двигателями при использовании плохо очищенного бензина и топками, в которых сгорают серосодержащие угли, торф или мазут. Ежегодно в атмосферу из-за сжигания угля и нефти выбрасываются миллионы тонн диоксида серы.
В природе диоксид серы встречается в вулканических газах. Диоксид серы окисляется кислородом воздуха в триоксид серы, который, поглощая воду (пары), превращается в серную кислоту. Выпадающие кислотные дожди разрушают цементные части построек, памятники архитектуры, высеченные из камня скульптуры. Кислотные дожди замедляют рост растений и даже приводят к их гибели, убивают живые организмы водоемов. Такие дожди вымывают из пашен малорастворимые в воде фосфорные удобрения, которые, попадая в водоемы, приводят к бурному размножению водорослей и быстрому заболачиванию прудов, рек.
Диоксид серы – бесцветный газ с резким запахом. Получать диоксид серы и работать с ним следует под тягой.
Сернистый газ можно получить, поместив в колбу,
закрывающуюся пробкой с отводной трубкой и
капельной воронкой, 5–10 г сульфита натрия. Из
капельной воронки с 10 мл концентрированной
серной кислоты (крайняя осторожность!)
приливайте ее по каплям к кристаллам сульфита
натрия. Вместо кристаллического сульфита натрия
можно воспользоваться его насыщенным раствором.
Диоксид серы можно получить также реакцией между
металлической медью и серной кислотой. В
круглодонную колбу, снабженную пробкой с
газоотводной трубкой и капельной воронкой,
положите медные стружки или куски проволоки и
прилейте из капельной воронки немного серной
кислоты (на 10 г меди берется около 6 мл
концентрированной серной кислоты). Для начала
реакции слегка нагрейте колбу. После этого
кислоту приливайте по каплям. Напишите уравнения
приема и отдачи электронов и суммарное
уравнение.
Свойства диоксида серы можно изучать, пропуская
газ через раствор реагента, или в виде водного
раствора (сернистой кислоты). Такие же результаты
получаются при использовании подкисленных
растворов сульфитов натрия Na 2 SO 3 и
калия К 2 SO 3 . В одном объеме воды
растворяется до сорока объемов сернистого газа
(получается ~6%-й раствор).
Диоксид серы токсичен. При легких отравлениях
начинается кашель, насморк, появляются слезы,
начинается головокружение. Увеличение дозы
приводит к остановке дыхания.
4а. Взаимодействие сернистой кислоты с пероксидом водорода.
Предскажите продукты взаимодействия сернистой
кислоты и пероксида водорода. Проверьте свое
предположение опытом.
К 2–3 мл сернистой кислоты прилейте столько же
3%-го раствора пероксида водорода. Как доказать
образование предполагаемых продуктов реакции?
Тот же опыт повторите с подкисленным и щелочным
растворами сульфита натрия.
Напишите уравнения реакций и рассчитайте ЭДС
процесса.
Выберите нужные вам электродные потенциалы:

4б. Реакция между сернистым газом и сероводородом.
Эта реакция проходит между газообразными SO 2
и H 2 S и служит для получения серы. Реакция
интересна также тем, что два загрязнителя
атмосферы взаимно уничтожают друг друга.
Проходит ли эта реакция между растворами
сероводорода и сернистого газа? Ответьте на этот
вопрос опытом.
Выберите электродные потенциалы для определения
возможности прохождения реакции в растворе:

Попробуйте провести термодинамический расчет возможности прохождения реакций. Термодинамические характеристики веществ для определения возможности прохождения реакции между газообразными веществами следующие:
При каком состоянии веществ – газообразном или в растворе – реакции более предпочтительны?
Пособие-репетитор по химии
Продолжение. Cм. в № 22/2005;
1, 2, 3, 5, 6, 8, 9, 11, 13, 15, 16, 18, 22/2006;
3, 4, 7, 10, 11, 21/2007;
2, 7, 11, 18, 19, 21/2008;
1, 3, 10/2009
ЗАНЯТИЕ 30
10-й класс (первый год обучения)
Сера и ее соединения
1. Положение в таблице Д.И.Менделеева, строение атома.
2. Происхождение названия.
3. Физические свойства.
4. Химические свойства.
5. Нахождение в природе.
6. Основные методы получения.
7. Важнейшие соединения серы (сероводород, сероводородная кислота и ее соли; сернистый газ, сернистая кислота и ее соли; триоксид серы, серная кислота и ее соли).
В периодической системе сера находится в главной подгруппе VI группы (подгруппа халькогенов). Электронная формула серы 1s 2 2s 2 p 6 3s 2 p 4 , это р -элемент. В зависимости от состояния сера может проявлять валентность II, IV или VI:
S: 1s 2 2s 2 2p 6 3s 2 3p 4 3d 0 (валентность II),
S * : 1s 2 2s 2 2p 6 3s 2 3p 3 3d 1 (валентность IV),
S ** : 1s 2 2s 2 2p 6 3s 1 3p 3 3d 2 (валентность VI).
Характерные степени окисления серы –2, +2, +4, +6 (в дисульфидах, содержащих мостиковую связь –S–S– (например, FeS 2), степень окисления серы равна –1); в соединениях входит в состав анионов, с более электроотрицательными элементами – в состав катионов, например:
Сера – элемент с высокой электроотрицательностью, проявляет неметаллические (кислотные) свойства. Имеет четыре стабильных изотопа с массовыми числами 32, 33, 34 и 36. Природная сера на 95 % состоит из изотопа 32 S.
Русское название серы произошло от санскритского слова cira – светло-желтый, по цвету природной серы. Латинское название sulfur переводится как «горючий порошок». 1
Ф и з и ч е с к и е с в о й с т в а
Сера образует три аллотропные модификации : ромбическая (-сера), моноклинная (-сера) и пластическая , или каучукоподобная. Наиболее устойчива при обычных условиях ромбическая сера, а выше 95,5 °С стабильна моноклинная сера. Обе эти аллотропные модификации имеют молекулярную кристаллическую решетку, построенную из молекул состава S 8 , расположенных в пространстве в виде короны; атомы соединены одинарными ковалентными связями. Различие ромбической и моноклинной серы состоит в том, что в кристаллической решетке молекулы упакованы по-разному.
Если ромбическую или моноклинную серу нагреть до точки кипения (444,6 °С) и полученную жидкость вылить в холодную воду, то образуется пластическая сера, по свойствам напоминающая резину. Пластическая сера состоит из длинных зигзагообразных цепей. Эта аллотропная модификация неустойчива и самопроизвольно превращается в одну из кристаллических форм.
Ромбическая сера – твердое кристаллическое вещество желтого цвета; в воде не растворяется (и не смачивается), но хорошо растворяется во многих органических растворителях (сероуглерод, бензол и т.д.). Сера обладает очень плохой электро- и теплопроводностью. Температура плавления ромбической серы +112,8 °С, при температуре 95,5 °С ромбическая сера переходит в моноклинную:
![]()
Х и м и ч е с к и е с в о й с т в а
По своим химическим свойствам сера является типичным активным неметаллом. В реакциях может быть как окислителем, так и восстановителем.
![]()
Металлы (+):
2Na + S = Na 2 S,
2Al + 3S Al 2 S 3 ,
Неметаллы (+/–)*:
2P + 3S P 2 S 3 ,
S + Cl 2 = SCl 2 ,
S + 3F 2 = SF 6 ,
S + N 2 реакция не идет.
Н 2 О (–). сера не смачивается водой.
Основные оксиды (–).
Кислотные оксиды (–).
Основания (+/–):
S + Cu(OH) 2 реакция не идет.
Кислоты (не окислители) (–).
Кислоты-окислители (+):
S + 2H 2 SO 4 (конц.) = 3SO 2 + 2H 2 O,
S + 2HNO 3 (разб.) = H 2 SO 4 + 2NO,
S + 6HNO 3 (конц.) = H 2 SO 4 + 6NO 2 + 2H 2 O.
В п р и р о д е сера встречается как в самородном состоянии, так и в виде соединений, важнейшими из которых являются пирит, он же железный, или серный, колчедан (FeS 2), цинковая обманка (ZnS), свинцовый блеск (PbS), гипс (CaSO 4 2H 2 O), глауберова соль (Na 2 SO 4 10H 2 O), горькая соль (MgSO 4 7H 2 O). Кроме того, сера входит в состав каменного угля, нефти, а также в различные живые организмы (в составе аминокислот). В организме человека сера концентрируется в волосах.
В л а б о р а т о р н ы х у с л о в и я х серу можно получить, используя окислительно-восстановительные реакции (ОВР), например:
H 2 SO 3 + 2H 2 S = 3S + 3H 2 O,
2H 2 S + O 2 2S + 2H 2 O.
В а ж н е й ш и е с о е д и н е н и я с е р ы
Сероводород (H 2 S) – бесцветный газ с удушающим неприятным запахом тухлых яиц, ядовит (соединяется с гемоглобином крови, образуя сульфид железа). Тяжелее воздуха, малорастворим в воде (2,5 объема сероводорода в 1 объеме воды). Связи в молекуле ковалентные полярные, sp 3 -гибридизация, молекула имеет угловое строение:
В химическом отношении сероводород достаточно активен. Он термически неустойчив; легко сгорает в атмосфере кислорода или на воздухе; легко окисляется галогенами, диоксидом серы или хлоридом железа(III); при нагревании взаимодействует с некоторыми металлами и их оксидами, образуя сульфиды:
![]()
2H 2 S + O 2 2S + 2H 2 O,
2H 2 S + 3O 2 2SO 2 + 2H 2 O,
H 2 S + Br 2 = 2HBr + S,
2H 2 S + SO 2 3S + 2H 2 O,
2FeCl 3 + H 2 S = 2FeCl 2 + S + 2HCl,
H 2 S + Zn ZnS + H 2 ,
H 2 S + CaO CaS + H 2 O.
В лабораторных условиях сероводород получают действием на сульфиды железа или цинка сильных минеральных кислот или необратимым гидролизом сульфида алюминия:
ZnS + 2HCl = ZnCl 2 + H 2 S,
Аl 2 SO 3 + 6HOH 2Al(OH) 3 + 3H 2 S.
Раствор сероводорода в воде – сероводородная вода, или сероводородная кислота . Слабый электролит, по второй ступени практически не диссоциирует. Как двухосновная кислота образует два типа солей – сульфиды и гидросульфиды :
например, Na 2 S – сульфид натрия, NaHS – гидросульфид натрия.
Сероводородная кислота проявляет все общие свойства кислот. Кроме того, сероводород, сероводородная кислота и ее соли проявляют сильную восстановительную способность. Например:
H 2 S + Zn = ZnS + H 2 ,
H 2 S + CuO = CuS + H 2 O,

Качественной реакцией на сульфид-ион является взаимодействие с растворимыми солями свинца; при этом выпадает осадок сульфида свинца черного цвета:
Pb 2+ + S 2– -> PbS,
Pb(NO 3) 2 + Na 2 S = PbS + 2NaNO 3 .
Оксид серы(IV) SO 2 – сернистый газ, сернистый ангидрид – бесцветный газ с резким запахом, ядовит. Кислотный оксид. Связи в молекуле ковалентные полярные, sp 2 -гибридизация. Тяжелее воздуха, хорошо растворим в воде (в одном объеме воды – до 80 объемов SO 2), образует при растворении сернистую кислоту , существующую только в растворе:
H 2 O + SO 2 H 2 SO 3 .
По кислотно-основным свойствам сернистый газ проявляет свойства типичного кислотного оксида, сернистая кислота также проявляет все типичные свойства кислот:
SO 2 + CaO CaSO 3 ,

H 2 SO 3 + Zn = ZnSO 3 + H 2 ,

H 2 SO 3 + CaO = CaSO 3 + H 2 O.
По окислительно-восстановительным свойствам сернистый газ, сернистая кислота и сульфиты могут проявлять окислительно-восстановительную двойственность (с преобладанием восстановительных свойств). С более сильными восстановителями соединения серы(IV) ведут себя как окислители:
![]()
С более сильными окислителями они проявляют восстановительные свойства:
![]()
В промышленности диоксид серы получают:
При горении серы:
Обжигом пирита и других сульфидов:
4FeS 2 + 11O 2 2Fe 2 O 3 + 8SO 2 ,
2ZnS + 3O 2 2ZnO + 2SO 2 .
К лабораторным методам получения относятся:
Действие сильных кислот на сульфиты:
Na 2 SO 3 + 2HCl = 2NaCl + SO 2 + H 2 O;
Взаимодействие концентрированной серной кислоты с тяжелыми металлами:
Cu + 2H 2 SO 4 (конц.) = СuSO 4 + SO 2 + 2H 2 O.
Качественные реакции на сульфит-ион – обесцвечивание «йодной воды» или действие сильных минеральных кислот:
Na 2 SO 3 + I 2 + 2NaOH = 2NaI + Na 2 SO 4 + H 2 O,
Ca 2 SO 3 + 2HCl = CaCl 2 + H 2 O + SO 2 .
Оксид серы(VI) SO 3 – триоксид серы, или серный ангидрид , – это бесцветная жидкость, которая при температуре ниже 17 °С превращается в белую кристаллическую массу. Ядовит. Существует в виде полимеров (мономерные молекулы существуют только в газовой фазе), связи в молекуле ковалентные полярные, sp 2 -гибридизация. Гигроскопичен, термически неустойчив. С водой реагирует с сильным экзо-эффектом. Реагирует с безводной серной кислотой, образуя олеум . Образуется при окислении сернистого газа:
![]()
SO 3 + H 2 O = H 2 SO 4 + Q ,
n n SO 3 .
По кислотно-основным свойствам является типичным кислотным оксидом:
SO 3 + H 2 O = H 2 SO 4 ,
SO 3 + CaO = CaSO 4 ,

По окислительно-восстановительным свойствам выступает сильным окислителем, обычно восстанавливаясь до SO 2 или сульфитов:
![]()
В чистом виде практического значения не имеет, является промежуточным продуктом при производстве серной кислоты.
Серная кислота – тяжелая маслянистая жидкость без цвета и запаха. Хорошо растворима в воде (с большим экзо-эффектом). Гигроскопична, ядовита, вызывает сильные ожоги кожи. Является сильным электролитом. Серная кислота образует два типа солей: сульфаты и гидросульфаты , которые проявляют все общие свойства солей. Сульфаты активных металлов термически устойчивы, а сульфаты других металлов разлагаются даже при небольшом нагревании:
Na 2 SO 4 не разлагается,
ZnSO 4 ZnO + SO 3 ,
4FeSO 4 2Fe 2 O 3 + 4SO 2 + O 2 ,
Ag 2 SO 4 2Ag + SO 2 + O 2 ,
HgSO 4 Hg + SO 2 + O 2 .
Раствор с массовой долей серной кислоты ниже 70 % обычно считается разбавленным; выше 70 % – концентрированным; раствор SO 3 в безводной серной кислоте называется олеум (концентрация триоксида серы в олеуме может достигать 65 %).
Разбавленная серная кислота проявляет все свойства, характерные для сильных кислот:
Н 2 SO 4 2H + + SO 4 2– ,
Н 2 SO 4 + Zn = ZnSO 4 + Н 2 ,
Н 2 SO 4 (разб.) + Cu реакция не идет,
Н 2 SO 4 + CaO = CaSO 4 + H 2 O,

CaCO 3 + Н 2 SO 4 = CaSO 4 + H 2 O + CO 2 .
Концентрированная серная кислота является сильным окислителем, особенно при нагревании. Она окисляет многие металлы, неметаллы, а также некоторые органические вещества. Не окисляются под действием концентрированной серной кислоты железо, золото и металлы платиновой группы (правда, железо хорошо растворяется при нагревании в умеренно концентрированной серной кислоте с массовой долей 70 %). При взаимодействии концентрированной серной кислоты с другими металлами образуются сульфаты и продукты восстановления серной кислоты.
2Н 2 SO 4 (конц.) + Cu = CuSO 4 + SO 2 + 2H 2 O,

5Н 2 SO 4 (конц.) + 8Na = 4Na 2 SO 4 + H 2 S + 4H 2 O,
Н 2 SO 4 (конц.) пассивирует Fe, Al.
При взаимодействии с неметаллами концентрированная серная кислота восстанавливается до SO 2:
5Н 2 SO 4 (конц.) + 2Р = 2H 3 PO 4 + 5SO 2 + 2H 2 O,
2Н 2 SO 4 (конц.) + C = 2H 2 O + CO 2 + 2SO 2 .
Контактный метод получения серной кислоты состоит из трех стадий:
1) обжиг пирита:
4FeS 2 + 11O 2 2Fe 2 O 3 + 8SO 2 ;
2) окисление SO 2 в SO 3 в присутствии катализатора – оксида ванадия:
![]()
3) растворение SO 3 в серной кислоте с получением олеума:
SO 3 + H 2 O = H 2 SO 4 + Q ,
n SO 3 + H 2 SO 4 (конц.) = H 2 SO 4 n SO 3 .
Качественная реакция на сульфат-ион – взаимодействие с катионом бария, в результате чего выпадает белый осадок BaSO 4 .
Ba 2+ + SO 4 2– -> BaSO 4 ,
BaCl 2 + Na 2 SO 4 = BaSO 4 + 2NaCl.
Тест по теме «Сера и ее соединения»
1. Сера и кислород – это:
а) хорошие проводники электричества;
б) относятся к подгруппе халькогенов;
в) хорошо растворимы в воде;
г) имеют аллотропные модификации.
2. В результате реакции серной кислоты с медью можно получить:
а) водород; б) серу;
в) сернистый газ; г) сероводород.
3. Сероводород – это:
а) ядовитый газ;
б) сильный окислитель;
в) типичный восстановитель;
г) один из аллотропов серы.
4. Массовая доля (в %) кислорода в серном ангидриде равна:
а) 50; б) 60; в) 40; г) 94.
5. Оксид серы(IV) является ангидридом:
а) серной кислоты;
б) сернистой кислоты;
в) сероводородной кислоты;
г) тиосерной кислоты.
6. На сколько процентов уменьшится масса гидросульфита калия после прокаливания?
в) гидросульфит калия термически устойчив;
7. Сместить равновесие в сторону прямой реакции окисления сернистого газа в серный ангидрид можно:
а) используя катализатор;
б) увеличивая давление;
в) уменьшая давление;
г) понижая концентрацию оксида серы(VI).
8. При приготовлении раствора серной кислоты необходимо:
а) наливать кислоту в воду;
б) наливать воду в кислоту;
в) порядок приливания не имеет значения;
г) серная кислота не растворяется в воде.
9. Какую массу (в г) декагидрата сульфата натрия необходимо добавить к 100 мл 8%-го раствора сульфата натрия (плотность равна 1,07 г/мл), чтобы удвоить массовую долю соли в растворе?
а) 100; б) 1,07; в) 30,5; г) 22,4.
10. Для определения сульфит-иона в качественном анализе можно использовать:
а) катионы свинца;
б) «йодную воду»;
в) раствор марганцовки;
г) сильные минеральные кислоты.
Ключ к тесту
| б, г | в | а, в | б | б | г | б, г | а | в | б, г |
Задачи и упражнения на серу и ее соединения
Ц е п о ч к и п р е в р а щ е н и й
1. Сера -> сульфид железа(II) -> сероводород -> сернистый газ -> триоксид серы > серная кислота > оксид серы(IV).
3. Серная кислота -> сернистый газ -> сера -> диоксид серы -> триоксид серы -> серная кислота.
4. Сернистый ангидрид -> сульфит натрия -> гидросульфит натрия -> сульфит натрия -> сульфат натрия.
5. Пирит -> сернистый газ -> серный ангидрид -> серная кислота -> оксид серы(IV) -> сульфит калия -> сернистый ангидрид.
6. Пирит > сернистый газ -> сульфит натрия -> сульфат натрия -> сульфат бария -> сульфид бария.
7. Сульфид натрия -> А -> В -> С -> D -> сульфат бария (все вещества содержат серу; первая, вторая и четвертая реакции – ОВР).
| У р о в е н ь А |
1. Через раствор, содержащий 5 г едкого натра, пропустили 6,5 л сероводорода. Определите состав полученного раствора.
Ответ. 7 г NaHS, 5,61 г H 2 S.
2. Какую массу глауберовой соли необходимо добавить к 100 мл 8%-го раствора сульфата натрия (плотность раствора равна 1,07 г/мл), чтобы удвоить массовую долю вещества в растворе?
Ответ. 30,5 г Na 2 SO 4 10H 2 O.
3. К 40 г 12%-го раствора серной кислоты добавили 4 г серного ангидрида. Вычислите массовую долю вещества в образовавшемся растворе.
Ответ. 22 % H 2 SO 4 .
4. Смесь сульфида железа(II) и пирита, массой 20,8 г, подвергли длительному обжигу, при этом образовалось 6,72 л газообразного продукта (н.у.). Определите массу твердого остатка, образовавшегося при обжиге.
Ответ. 16 г Fe 2 O 3 .
5. Имеется смесь меди, углерода и оксида железа(III) с молярным соотношением компонентов 4:2:1 (в порядке перечисления). Какой объем 96%-й серной кислоты (плотность равна 1,84 г/мл) нужен для полного растворения при нагревании 2,2 г такой смеси?
Ответ. 4,16 мл раствора H 2 SO 4 .
6. Для окисления 3,12 г гидросульфита щелочного металла потребовалось добавить 50 мл раствора, в котором молярные концентрации дихромата натрия и серной кислоты равны 0,2 моль/л и 0,5 моль/л соответственно. Установите состав и массу остатка, который получится при выпаривании раствора после реакции.
Ответ . 7,47 г смеси сульфатов хрома (3,92 г) и натрия (3,55 г).
| У р о в е н ь Б |
(задачи на олеум)
1. Какую массу триоксида серы надо растворить в 100 г 91%-го раствора серной кислоты, чтобы получить 30%-й олеум?
Решение
По условию задачи:
m (H 2 SO 4) = 100 0,91 = 91 г,
m (H 2 O) = 100 0,09 = 9 г,
(H 2 O) = 9/18 = 0,5 моль.
Часть добавленного SO 3 (m 1) пойдет на реакцию с H 2 O:
H 2 O + SO 3 = H 2 SO 4 .
По уравнению реакции:
(SO 3) = (H 2 O) = 0,5 моль.
m 1 (SO 3) = 0,5 80 = 40 г.
Вторая часть SO 3 (m 2) пойдет на создание концентрации олеума. Выразим массовую долю олеума:

m 2 (SO 3) = 60 г.
Суммарная масса триоксида серы:
m (SO 3) = m 1 (SO 3) + m 2 (SO 3) = 40 + 60 = 100 г.
Ответ . 100 г SO 3 .
2. Какую массу пирита необходимо взять для получения такого количества оксида серы(VI), чтобы, растворив его в 54,95 мл 91%-го раствора серной кислоты (плотность равна 1,82 г/см 3), получить 12,5%-й олеум? Выход серного ангидрида считать за 75 %.
Ответ . 60 г FeS 2 .
3. На нейтрализацию 34,5 г олеума расходуется 74,5 мл 40%-го раствора гидроксида калия (плотность равна 1,41 г/мл). Сколько молей серного ангидрида приходится на 1 моль серной кислоты в этом олеуме?
Ответ . 0,5 моль SO 3 .
4. При добавлении оксида серы(VI) к 300 г 82%-го раствора серной кислоты получен олеум с массовой долей триоксида серы 10%. Найдите массу использованного серного ангидрида.
Ответ . 300 г SO 3 .
5. При добавлении 400 г триоксида серы к 720 г водного раствора серной кислоты получен олеум с массовой долей 7,14 %. Найдите массовую долю серной кислоты в исходном растворе.
Ответ . 90 % H 2 SO 4 .
6. Найдите массу 64%-го раствора серной кислоты, если при добавлении к этому раствору 100 г триоксида серы получается олеум, содержащий 20 % триоксида серы.
Ответ . 44,4 г раствора H 2 SO 4 .
7. Какие массы триоксида серы и 91%-го раствора серной кислоты необходимо смешать для получения 1 кг 20%-го олеума?
Ответ . 428,6 г SO 3 и 571,4 г раствора H 2 SO 4 .
8. К 400 г олеума, содержащего 20 % триоксида серы, добавили 100 г 91%-го раствора серной кислоты. Найдите массовую долю серной кислоты в полученном растворе.
Ответ . 92 % H 2 SO 4 в олеуме.
9. Найдите массовую долю серной кислоты в растворе, полученном при смешивании 200 г 20%-го олеума и 200 г 10%-го раствора серной кислоты.
Ответ . 57,25 % H 2 SO 4 .
10. Какую массу 50%-го раствора серной кислоты необходимо добавить к 400 г 10%-го олеума для получения 80%-го раствора серной кислоты?
Ответ . 296,67 г 50%-го раствора H 2 SO 4 .
Ответ . 114,83 г олеума.
К а ч е с т в е н н ы е з а д а ч и
1. Бесцветный газ А с резким характерным запахом окисляется кислородом в присутствии катализатора в соединение В, представляющее собой летучую жидкость. Вещество В, соединяясь с негашеной известью, образует соль С. Идентифицируйте вещества, напишите уравнения реакций.
Ответ . Вещества: А – SO 2 , B – SO 3 , C – CaSO 4 .
2. При нагревании раствора соли А образуется осадок В. Этот же осадок образуется при действии щелочи на раствор соли А. При действии кислоты на соль А выделяется газ С, обесцвечивающий раствор перманганата калия. Идентифицируйте вещества, напишите уравнения реакций.
Ответ . Вещества: А – Ca(HSO 3) 2 , B – CaSO 3 , C – SO 2 .
3. При окислении газа А концентрированной серной кислотой образуется простое вещество В, сложное вещество С и вода. Растворы веществ А и С реагируют между собой с образованием осадка вещества В. Идентифицируйте вещества, напишите уравнения реакций.
Ответ . Вещества: А – H 2 S, B – S, C – SO 2 .
4. В реакции соединения двух жидких при обычной температуре оксидов А и В образуется вещество С, концентрированный раствор которого обугливает сахарозу. Идентифицируйте вещества, напишите уравнения реакций.
Ответ . Вещества: А – SO 3 , B – H 2 O, C – H 2 SO 4 .
5. В вашем распоряжении имеются сульфид железа(II), сульфид алюминия и водные растворы гидроксида бария и хлороводорода. Получите из этих веществ семь различных солей (без использования ОВР).
Ответ . Соли: AlCl 3 , BaS, FeCl 2 , BaCl 2 , Ba(OH)Cl, Al(OH)Cl 2 , Al(OH) 2 Cl.
6. При действии концентрированной серной кислоты на бромиды выделяется сернистый газ, а на йодиды – сероводород. Напишите уравнения реакций. Объясните разницу в характере продуктов в этих случаях.
Ответ . Уравнения реакций:
2H 2 SO 4 (конц.) + 2NaBr = SO 2 + Br 2 + Na 2 SO 4 + 2H 2 O,
5H 2 SO 4 (конц.) + 8NaI = H 2 S + 4I 2 + 4Na 2 SO 4 + 4H 2 O.
1 См.: Лидин Р.А. «Справочник по общей и неорганической химии». М.: Просвещение, 1997.
* Знак +/– означает, что данная реакция протекает не со всеми реагентами или в специфических условиях.
Продолжение следует






Соблазнённая, но не покинутая
Эстонская ведьма с 'Битвы экстрасенсов'
Когда и как подавать документы в вуз
Очерк политической истории Сирии в ХХ и начале ХХI века Какие нации и религии живут в сирии
С какой скоростью читал ленин